Kita mengenal suatu zat sebagai Asam dan Basa berdasarkan derajat pH nya. Istilah “pH” berasal dari kata Jerman “potenz,” yang berarti “pangkat” , dikombinasikan dengan H, simbol unsur untuk hidrogen, jadi pH adalah singkatan dari “pangkat hidrogen.” Pengertian pada umumnya, pH (Power of Hydrogen) adalah skala yang digunakan untuk menyatakan tingkat keasaman atau kebasaan yang dimiliki oleh suatu larutan. Skala dari pH terdiri dari angka 1 hingga 14. Skala pH menunjukkan konsentrasi ion hidrogen [H+] dalam larutan. Nilai pH larutan dihitung menggunakan nilai konsentrasi molar ion hidrogen yang larut dalam larutan.
Berikut merupakan skala pH ditinjau hubungannya dengan derajat asam basa sebuah benda:

Untuk menentukan suatu zat atau molekul tergolong ASAM maupun BASA setidaknya ada tiga konsep yang sudah dikembangkan yaitu:
1. Teori Arhenius
Asam : menghasilkan ion H+ dalam air
Basa : menghasilkan ion OH- dalam air
Contoh:

2. Teori Bronsted Lowry
Asam : Donor/pemberi proton (H)
Basa : Akseptor/penerima proton (H)
Contoh:
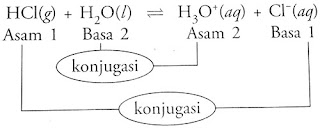
Dari reaksi tersebut
HCl dan H3O+ tergolong ASAM
H2O dan Cl– tergolong BASA
HCl dan Cl– Merupakan ASAM BASA KONJUGASI
H2O dan H3O+ Merupakan ASAM BASA KONJUGASI
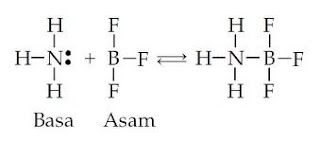
3. Teori Lewis
Asam : Akseptor pasangan elektron (PE)
Basa : Penerima pasangan elektron (PE)
Contoh:
BF3 merupakan ASAM karena ia menerima PE dari NH3
NH3 merupakan BASA karena ia memberi PE kepada BF3
Berikut ini merupakan tabel daftar ASAM dan BASA yang harus kamu ketahui:
TABEL ASAM DAN BASA KUAT
|
ASAM KUAT |
BASA KUAT |
|
Asam Klorida (HCl)
Asam Sulfat (H2SO4)
Asam Nitrat (HNO3)
Asam Bromida (HBr)
Asam Iodida (HI)
Asam Klorat (HClO3)
Asam Perklorat (HClO4)
|
Litium Hidroksida (LiOH)
Natrium Hidroksida (NaOH)
Kalium Hidroksida (KOH)
Berilium Hidroksida (Be(OH)2)
Magnesium Hidroksida (Mg(OH)2)
Kalsium Hidroksida (Ca(OH)2)
Barium Hidroksida (Ba(OH)2)
|
TABEL ASAM DAN BASA LEMAH
|
ASAM LEMAH |
BASA LEMAH |
|
Asam Asetat (CH3COOH)
Asam Fospat (H3PO4)
Asam Fospit (H2PO4)
Asam Nitrit (HNO2)
Asam Format (HCOOH)
Asam Sitrat (C6H8O7)
Asam Fluorida (HF)
Asam Karbonat (H2CO3)
Asam Sianida (HCN)
Asam Borat (H2BO3)
Asam Silikat (H2SiO3)
Asam Oksalat (H2C2O4)
Asam Benzoat (C6H5COOH)
Asam Sulfit (H2SO3)
Asam Sulfida (H2S)
Asam Hipoklorit (HClO)
Asam Arsenit (H3AsO3)
Asam Arsenat (H3AsO4)
Asam Laktat (C3H5O3)
Asam Antimonit (H2SbO3)
Asam Antimonat (H2SbO4)
|
Amonium Hidroksida (NH4OH)
Aluminium Hidroksida (Al(OH)3)
Besi (III) Hidroksida (Fe(OH)3)
Besi (II) Hidroksida (Fe(OH)2)
Karbosium Hidroksida (CA(OH)3)
Nikel Hidroksida (Ni(OH)2)
Seng Hidroksida (Zn(OH)2)
Kadmium Hidroksida (Cd(OH)2)
Bismut Hidroksida (Bi(OH)3)
Perak Hidroksida (AgOH)
Emas (I) Hidroksida (Au(OH))
Emas (III) Hidroksida (Au(OH)3)
Tembaga (I) Hidroksida (Cu(OH)2)
Tembaga (II) Hidroksida (Cu(OH))
Raksa (I) Hidroksida (Hg(OH))
Raksa (II) Hidroksida (Hg(OH)2)
Timah (II) Hidroksida (Sn(OH)2)
Timah (IV) Hidroksida (Sn(OH)4)
Timbal (II) Hidroksida (Pb(OH)2)
Mangan Hidroksida (Mn(OH)2)
Kobalt (III) Hidroksida (Co(OH)3)
Kobalt (II) Hidroksida (Co(OH)2)
Anilia (C6H5NH2)
Dimetilamina ((CH3)2 NH)
Metil hidroksida (CH3OH) |
Bersambung PART 2
Cara menghitung pH larutan ASAM & BASA: KLIK DISINI